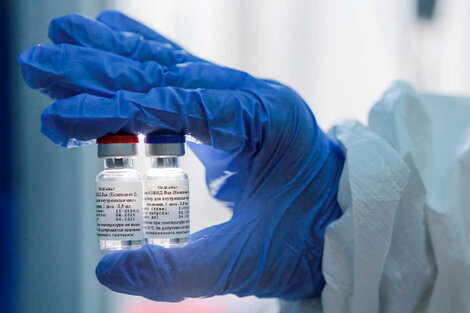
El ministro de Salud de Rusia, Mijaíl Murashko, anunció que la próxima semana comenzarán las entregas de la vacuna Sputnik V a clínicas médicas. Además, confirmó que en paralelo iniciarán la fase 3 de los ensayos clínicos de la que participarán 40.000 personas.
"Esta semana comenzará la vacunación de aquellos voluntarios que participarán en la fase 3 de los ensayos clínicos, y en paralelo la semana que viene comenzarán las primeras entregas de la vacuna, pequeñas por ahora, porque se deben cumplir todos los intereses. Esta semana anunciaremos definitivamente todas las fechas", afirmó Murashko.
Los ensayos correspondientes a la fase 3 se llevarán a cabo en varias instituciones médicas estatales de Moscú. De esta etapa participarán 40.000 personas y 10.000 de ellas recibirán un placebo. La participación de cada voluntario tendrá una duración de seis meses a partir del día en que reciba la vacuna. El alcalde de la ciudad, Sergei Sobyanin, sostuvo que está lista toda la infraestructura para realizar los estudios.
Sobyanin también precisó que ya hay 5 mil personas inscritas para recibir la vacuna Sputnik V. La vicealcaldesa moscovita, Anastasia Rakova, informó el viernes pasado que el primer lote de vacunas ya había llegado a tres policlínicos de la capital rusa.
El avance de la vacuna Sputnik V
La vacuna Sputnik V fue registrada el 11 de agosto y recibió críticas -que Murashko calificó como "infundadas"- a nivel internacional por no haber difundido los resultados de los ensayos clínicos en revistas de la comunidad científica. Finalmente, la revista médica The Lancet publicó los resultados de las fases 1 y 2 de la vacuna contra el coronavirus desarrollada por el Centro Nacional de Investigación de Epidemiología y Microbiología Gamaleya.
A fines de agosto, Kirill Dmitriev, CEO del Fondo de Inversión Directa de Rusia (FIDR), y los científicos del Centro de Investigación Gamaleya, Alexander Gintsburg y Denis Logunov, dieron una conferencia de prensa para brindar información sobre la vacuna. Logunov precisó que en los ensayos clínicos de las fases 1 y 2, que se completaron el 1 de agosto, la vacuna “demostró altos niveles de seguridad” y que genera “una alta respuesta inmunológica”.
Según Logunov, durante la investigación "no se reportaron efectos secundarios graves" -sólo dolores de cabeza o molestias por el pinchazo de la jeringa- y todos los voluntarios “desarrollaron anticuerpos neutralizantes del virus".