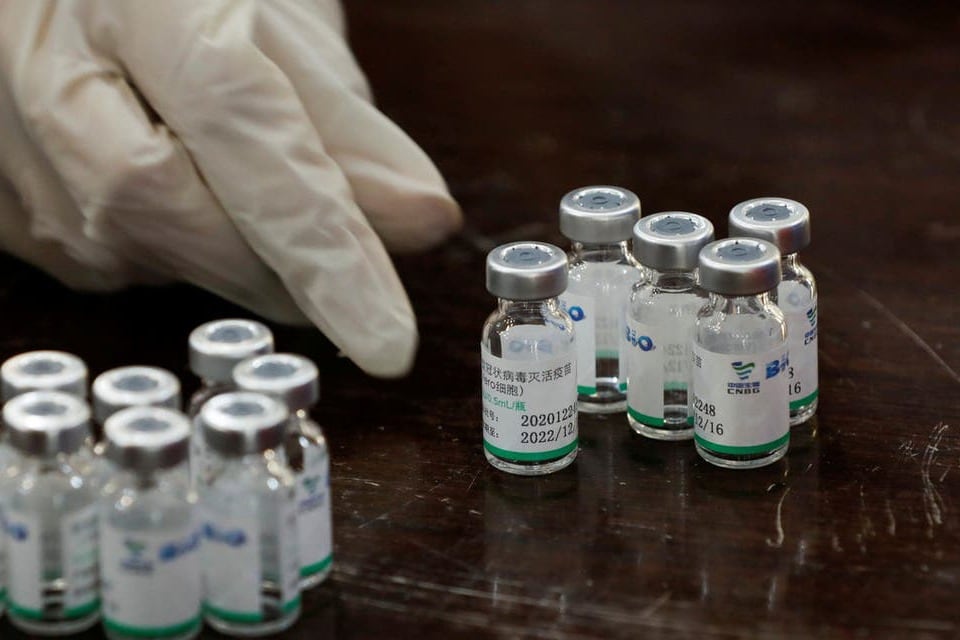
Es de una sola dosis y tiene una eficacia del 95 por ciento para casos graves
Cansino: cómo funciona la vacuna que llegará al país
La vacuna contra la covid-19 Convidecia, desarrollada por el laboratorio chino Cansino Biologics INC., es de una sola dosis, lo cual permite acelerar el ritmo de las inoculacio